per Kreditkarte, Paypal und Banküberweisung.
mit BRT-, DPD- und FedEx-Kuriern
per WhatsApp + 39.371.43.61.201
Der perineale Elektrostimulator BECA 28UG ist ein therapeutisches Gerät zur Behandlung von Inkontinenz mittels perinealer Elektrostimulation für den beruflichen oder persönlichen Gebrauch.
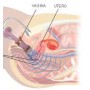
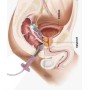
Die perineale Elektrostimulation Intellistim 28UG von BEAC mit vaginalen oder analen Sonden ist in vielen Fällen von Harninkontinenz die Behandlung der Wahl.
Entscheidend für den Therapieerfolg ist oft die Möglichkeit, die professionelle Behandlung durch Home-Sessions zu ergänzen.
Die IntelliSTIM UG-Einheit ist zwar mit ausgefeilten Funktionen und funktionaler Flexibilität ausgestattet, die für den professionellen Einsatz erforderlich sind, ist aber auch direkt vom Patienten einfach zu bedienen.
- Großes LCD-Display
- Einfach und intuitiv zu bedienen
- 4 kostenlose Programme
- 11 wählbare Programme, geeignet für verschiedene Inkontinenzbehandlungen.
- IntelliSTIM-Funktion mit interaktiver automatischer Anpassung von Zeitparametern
- Anzeige aller Parameter und Möglichkeit der Modifikation während der Sitzung
- 2 wählbare Wellenformen für die Verwendung mit Ring- oder Stabsonden.
Das Gerät ist in der Lage, eine Tibiastimulation zur Behandlung von Beckenproblemen durchzuführen, indem es die Alettrodes kauft.
Nicht-invasive transkutane Elektrostimulation bei der Behandlung der überaktiven Blase
Abstrakt
Wir überprüften die Literatur zur transkutanen elektrischen Nervenstimulation (TENS), die als Therapie für überaktive Blasensymptome (OAB) eingesetzt wird, mit besonderem Fokus auf: Stimulationsort, Stimulusparameter, neuronale Strukturen, von denen angenommen wird, dass sie anvisiert werden, und klinische und urodynamische Ergebnisse. In den meisten Studien wurde die Stimulation des Sakralnervs oder des Schienbeinnervs eingesetzt. Die Literatur deutet darauf hin, dass die TENS-Therapie zwar neuromodulatorische Wirkungen haben kann, es jedoch unwahrscheinlich ist, dass der Patient von einer einzigen Anwendung von TENS signifikant profitiert, und in der Tat wurden keine offensichtlichen Vorteile aus akuten Studien berichtet. In Langzeitstudien zeigten sich Unterschiede in der Beschreibung der Stimulationsintensität, der Therapiestrategie und der Elektrodenplatzierung sowie in den verschiedenen Symptomen und der Pathologie der Patienten. Darüber hinaus waren die meisten Studien unkontrolliert und bewerteten daher den Placebo-Effekt nicht. Über den grundlegenden Mechanismus, nach dem diese Therapien wirken, ist wenig bekannt und daher genau, welche Strukturen mit welchen Parametern stimuliert werden müssen. Es gibt vielversprechende Evidenz für die Wirksamkeit eines transkutanen Stimulationsansatzes, aber es ist eine angemessene Standardisierung der Stimulationskriterien und Ergebnismessungen erforderlich, um den besten Weg zur Behandlung dieser Therapie zu definieren und ihre Wirksamkeit zu dokumentieren.
1. Einleitung
Die Symptome des Syndroms der überaktiven Blase (OAB) sind eine bekannte Reihe von Symptomen, die der Patient während der Phase des Wasserlassens erlebt. Sie ist gekennzeichnet durch Harndrang (ein plötzlicher Harndrang, der nur schwer aufgeschoben werden kann), der bei fast allen Patienten mit einer erhöhten Häufigkeit und Nykturie und insbesondere bei weiblichen Patienten mit einer Dranginkontinenz einhergeht [1] . Etwa ein Drittel der Patientinnen ist durch Harninkontinenz stark gestört [2] .
Die Elektrostimulation wird seit mehreren Jahrzehnten bei der Behandlung verschiedener Funktionsstörungen der unteren Harnwege eingesetzt. Der Finetech-Bridley-Sakralstimulator etablierte die vordere Wurzel [3] , eine implantierte elektrische Sakralwurzel (S 2 -S 4 ) Stimulator zur Unterstützung der Blasenentleerung, bildete einen Vorläufer der heute weit verbreiteten sakralen Neuromodulationstechniken [4] und [5 ] . I S 2 -S 4 Nervenwurzeln versorgen die Blase mit motorischer Kraft. Insbesondere die S 3 Die Wurzel innerviert hauptsächlich den Detrusormuskel und ist das Hauptziel der sakralen Neuromodulation.
Ein weiterer wichtiger und gut etablierter Ort der Stimulation ist der hintere Nervus tibialis (PTN). Der PTN ist ein gemischter Nerv, der L 5 -S 3 Fasern, die wiederum aus den gleichen Wirbelsäulensegmenten stammen wie die parasympathischen Innervationen in die Blase (S 2 -S 4 ). Der afferente Stoller-Nervenstimulator (SANS) wurde eingeführt, um die PTN mit einer 34-Gauge-Elektrode zu stimulieren, die an der gleichen Stelle eingesetzt wird und in der Elektroakupunktur verwendet wird (der sogenannte SP6-Punkt), wobei eine Oberflächenelektrode hinter dem medialen Knöchel platziert wird [ 6] . Derzeit verwendet ein kommerzielles Gerät (Urgent-PC, Uroplasty, Inc., Minnetonka, USA) diese Technik. In der Regel werden 12 Sitzungen der posterioren perkutanen Tibianervenstimulation (PTNS) in wöchentlichen Abständen durchgeführt, und eine große randomisierte, placebokontrollierte Studie zeigte eine signifikante Verbesserung der allgemeinen OAB-Symptome (60/110) im Vergleich zu Scheinsymptomen (23/110) [7] . Es hat sich gezeigt, dass PTNS-Responder länger als 12 Monate von der Therapie profitieren können [8] . Der genaue Mechanismus des PTNS ist nach wie vor unklar, multidisziplinäre Studien und weitere Studien sind erforderlich, um dies aufzuklären.
Für die Zwecke dieser Übersicht werden wir nur nicht-invasive Techniken betrachten, definiert als "ein Verfahren, bei dem kein Instrument in den Körper eingeführt wird". Darüber hinaus definieren wir die transkutane elektrische Nervenstimulation (TENS) auch als eine Technik, bei der elektrische Reize durch intakte Haut geleitet werden.
Der Hauptgrund, sich auf diesen Modus zu konzentrieren, ist, dass er eine Reihe praktischer Vorteile bei der Bereitstellung bietet. Die Methode ist völlig nicht-invasiv, wobei Oberflächenelektroden an einer kostengünstigen Stimulatorbatterie befestigt und an einer geeigneten Stelle am Körper angebracht werden. Stimulatoren sind einfach zu bedienen, da die kostengünstigen, in der Regel auf Hydrogelen basierenden Elektroden und Batterien die einzigen Kosten für die laufende Behandlung darstellen. Die TENS-Behandlung selbst sollte keine regelmäßigen Patientenbesuche in Kliniken erfordern und wird in der Regel zu Hause selbst durchgeführt, was für den Patienten bequem ist. Im Allgemeinen gibt es wenig bis gar keine Nebenwirkungen zu Dutzenden, obwohl manchmal Rötungen oder Reizungen der Haut um die Elektroden auftreten können, die sich nach Beendigung der Stimulationssitzung auflösen. TENS wird seit mehreren Jahrzehnten auch zur Schmerzkontrolle eingesetzt. Der Einsatz von TENS bei der Behandlung von OAB und Erkrankungen der unteren Harnwege ist weniger etabliert.
- Abbildung 2.
Elektrodenposition für die transkutane Stimulation des Nervus tibialis posterior (TPTNS). Die Stimulation kann mit einem herkömmlichen Gerät zur transkutanen elektrischen Nervenstimulation (TENS) durchgeführt werden.
Andere minimal-invasive Elektrostimulationstechniken wie z.B.: Plugs, vaginale Analstimulation [9] und [10] ; perkutane Stimulation (die Nadel wird in der Nähe eines Zielnervs eingeführt); o implantierte Stimulationsgeräte liegen außerhalb des Rahmens dieser Überprüfung [4] und [5] . Insbesondere die Plugs werden vom Patienten oft aus Verlegenheit und einem Gefühl der Unreinheit abgelehnt [11] .
Der dorsale Genitalnerv wurde als weiterer Stimulationsort genutzt [10] Verwendung von Oberflächenelektroden zur Bereitstellung von Reizen. Da sich dieser Review jedoch auf Techniken konzentriert, die für Patienten geeignet sind, haben wir diese Studien nicht im Detail überprüft.
2. Methoden
Wir haben die elektronische Datenbank PubMed von Anfang an bis Dezember 2013 durchsucht. Die verwendeten Suchbegriffe waren "Dranginkontinenz", "Harndrang", "überaktive Blase", "Harninkontinenz" oder "Detrusorinstabilität" in Kombination mit "elektrische Stimulation", "tens", "tens", "nervenstimulation", "Neuromodulationsfläche", "nicht-invasive Stimulation", "Versuch" oder "Studie". Darüber hinaus folgten wir Zitaten aus Primärverweisen auf relevante Artikel, die die Datenbank nicht finden konnte. Ausschlusskriterien waren: Studien, die nicht in englischer Sprache verfasst waren; Studien zur Behandlung von Stuhlinkontinenz; solche, an denen Kinder beteiligt sind, solche, die Tiermodelle untersuchen; solche, die perkutane elektrische Stimulation, anale Stimulation, vaginale/penisartige Stimulation oder implantierte Geräte beinhalten oder solche, die sich nicht in erster Linie auf Speichersymptome konzentrieren. Ein Flussdiagramm des Auswahlprozesses ist in Abb. 1 dargestellt.
Abbildung 1.
Flussdiagramm des Papiersortierprozesses.
Optionen für Abbildungen
3. Ergebnisse
In der Primärforschung wurden 410 Items identifiziert. Anhand der definierten Ausschlusskriterien haben wir uns 16 Artikel im Detail angeschaut. Wir haben nicht speziell Studien mit einer höheren Konzentration auf interstitielle Zystitis oder invalide Dysfunktion überprüft, obwohl diese gegebenenfalls erwähnt werden.
3.1. Sakrale Stimulation
Im Jahr 1996 haben Hasan et al. [12] Respekt S 3 Neuromodulation mit implantierten Geräten mit TENS, die auf die perianale Region appliziert werden (S 2 -S 3 Dermome). Die Verbesserung bei mehr als 50 % der Patienten mit Detrusor-Idiopathie deutete auf das Potenzial der Verwendung von TENS an einer sakralen Stelle hin.
In einer Studie von Walsh et al. [13] 1 Woche ab kontinuierlicher Stimulation für 12 Stunden pro Tag bei S 3 Dermatome verbesserten sowohl die Häufigkeit als auch die Nykturie erheblich. Allerdings setzten nur 3/32 Patienten die Therapie fort, und das auch nur intermittierend, während einer Nachbeobachtungszeit von bis zu 6 Monaten. Die Autoren bewerteten nicht, ob Patienten, bei denen TENS für Tag 12 festgestellt wurde, es unangenehm war und möglicherweise zum Abbruch der Therapie führen kann.
Im Anschluss an diese Studie berichtete eine urodynamisch geschätzte Gruppe von 33 Patienten, die an Detrusor-Hyperaktivität und OAB-Symptomen litten, in einer 14-wöchigen Crossover-Studie (6 W Stimulation + 2 Auswaschung w + 6 w Stimulation) über eine selbst verabreichte Stimulation über das Sakralteil zweimal täglich im Vergleich zu Oxybutynin (6 W Stimulation + 2 Auswaschung w +6 w Stimulation) [14] . Die Stimulationsgruppe berichtete auch von weitaus weniger Nebenwirkungen in einem Oxybutynin-Vergleich. Die Autoren dokumentierten bei 30 % der Patienten nicht spezifisch einen gewissen Grad an Schwierigkeiten bei der Anwendung der Stimulation. Dies kann die Unannehmlichkeiten beim Platzieren von Elektroden auf S widerspiegeln 2 -S 3 Dermatome oder die Länge der täglichen Behandlungssitzung (bis zu 6 h).
Eine heterogene Gruppe von neurogenen Patienten mit Harnwegssymptomen wurde in einer nicht-randomisierten Studie mit einem TENS-Gerät mit Elektroden untersucht, die zweimal täglich in einer häuslichen Umgebung über den Geburtsschlitz gelegt wurden [15] . Neunzehn von 44 Patienten entschieden sich nach dieser Studie, das Gerät zu behalten, was mit der berichteten positiven Wirkung der Behandlung übereinstimmt.
Eine weitere kleine Studie mit 18 Patienten (7 neurogene Blase, 5 OAB, 6 Nykturie) berichtete über eine Verbesserung bei 10/18 nach 1-monatiger Stimulation des Foramen sacralis posterior [11] . Die Autoren schlugen vor, dass diese Art der Therapie weniger Beschwerden verursacht als die Stimulation der Vaginal- oder Analwirbelsäule. Im Widerspruch zu dieser Behauptung berichteten sie jedoch, dass in einigen Fällen die Intensität nicht hoch genug eingestellt war, um bei allen Patienten signifikante Wirkungen zu erzielen.
3.2. Stimulation des Nervus tibialis posterior (PTNS)
McGuire et al. [16] Zuerst wurde periphere elektrische Stimulation zur Stimulation von PTN eingesetzt. In dieser ersten Studie wurde eine Anodenelektrode auf dem Nervus peroneus communis (PTN) platziert und eine Kathodenelektrode über der kontralateralen äquivalenten Stelle. Sie berichteten über positive Ergebnisse bei 8/11-Patienten mit Detrusor-Hyperaktivität, die nach der Behandlung trocken wurden, und bei sieben Patienten mit neurologischen Erkrankungen (Multiple Sklerose, Rückenmarksverletzung), von denen fünf trocken wurden oder sich besserten. Im Anschluss daran wurde mit dem SANS und anschließend mit dem Urgent PC-Gerät eine substanzielle Evidenzbasis unter Verwendung des perkutanen Ansatzes zur Stimulation der PTN geschaffen, obwohl eine andere Stelle als in der ursprünglichen Beschreibung von McGuire et al. verwendet wurde. In weiteren Studien zur perkutanen oder transkutanen posterioren Tibianervenstimulation (TPTNS) wurden Elektroden verwendet, die auf der gleichen Fläche wie das SANS platziert wurden (Abb. 2) [6] . Daher könnte TPTNS eine plausible und potenziell attraktive Behandlungsoption sein, basierend auf der verfügbaren Evidenz für seine perkutane Wirksamkeit.
Abbildung 2.
Elektrodenposition für die transkutane Stimulation des Nervus tibialis posterior (TPTNS). Die Stimulation kann mit einem herkömmlichen Gerät zur transkutanen elektrischen Nervenstimulation (TENS) durchgeführt werden.
Optionen für Abbildungen
Die persönliche Wirksamkeit von TPTNS und Oxybutynin im Vergleich zur Kontrolle wurde bei 28 Frauen mit OAB untersucht [17] . Es wurde beschrieben, dass TPTNS die subjektiven Symptome ohne unerwünschte Ereignisse verbessert, aber robustere Bewertungsinstrumente und eine sorgfältige Dokumentation der Ätiopathologie der untersuchten Patienten wären erforderlich, um detailliertere Schlussfolgerungen zu ziehen.
Eine signifikante Verbesserung bei älteren Frauen mit Dranginkontinenz wurde nach 12 Wochen (einmal pro Woche) Stimulation in Kombination mit Kegel-Training und Blasenbildung berichtet [18] . Dieser Effekt war jedoch nicht besser als bei Patienten in einer Gruppe, die überhaupt keinen Stimulus erhielten.
In einer nicht randomisierten selbstverabreichten TPTNS-Studie berichteten 83 % der Patienten mit Multipler Sklerose (MS) über eine klinische Verbesserung im Notfall [19] . Diese Studie bestätigte auch eine gute Therapieakzeptanz der Patienten im familiären Umfeld.
In einer Placebo-Kontrollstudie wurden 37 Frauen mit Symptomen einer idiopathischen OAB randomisiert in eine Behandlungs- oder Scheingruppe mit Elektroden eingeteilt, die für beide Gruppen an der gleichen Stelle platziert wurden [20] . Stark verbesserte Harnfrequenz, sowohl in der Behandlungsgruppe ( p = 0,002) und in der Sham-Gruppe ( p = 0,025). Ein statistisch signifikanter Unterschied zwischen den Gruppen wurde nicht erreicht, ein möglicher Störfaktor war die ungleiche Ausgangshäufigkeit des Wasserlassens (13,88 Vs. 11,35 pro Tag).
3.3. Andere Orte der elektrischen Stimulation
Eine der ersten Techniken zur Behandlung von Low-Storage-Dysfunktion der stimulierten suprapubischen Harnwegsregion bei Patienten mit schmerzhaftem Blasensyndrom [21] und [22] . Diese Methode wurde zur Linderung von Bauchschmerzen eingesetzt, ähnlich dem Prinzip von TENS, wenn es angeblich zur Schmerzlinderung eingesetzt wird. In der Folge kam es bei diesen Patienten auch zu einer Verminderung der [22] . Zwei nachfolgende Studien dokumentierten eine Verbesserung der urodynamischen Parameter bei Patienten mit Detrusorhyperaktivität (DO), sensorischen Trieben oder neurogenen Problemen. Basierend auf der Literatur ist die Wirksamkeit der Stimulation einer suprapubischen Stelle bei Patienten mit OAB-Symptomen jedoch nicht nachgewiesen [23] und [24] .
Ein weiterer bekannter Ansatz hat die Stimulation der Oberschenkelmuskulatur bei Patienten mit Rückenmarksverletzungen eingesetzt, um die Spastik zu lindern. In einigen dieser Fälle hat dies zu einer Verbesserung der Dranginkontinenz geführt [25] und eine Erhöhung der maximalen Zystometriekapazität (MCC) und ein reduzierter maximaler Detrusordruck (MDP) [26] und [27] . Darüber hinaus berichteten 6/19 Patienten über eine klinische Verbesserung der Harninkontinenz, und die Häufigkeit erstreckt sich über 3 Monate nach der Behandlung [26] .
Basierend auf dieser, bestenfalls begrenzten Evidenz für eine Stimulation an anderen Stellen, scheint der logischste Ansatz für transkutane elektrische Stimulationstechniken ein sakraler Stimulus oder PTNS zu sein, da sie direkt oder indirekt angesprochen werden, die S 3 Rückenmarkswurzel.
3.4. Sind akute stimulierende Wirkungen von klinischer Bedeutung?
Ein naheliegender Ansatz zur Beantwortung dieser Frage wäre die Bewertung der Wirksamkeit der elektrischen Stimulation bei der Unterdrückung der Detrusor-Hyperaktivität (DO), die gewählt wurde, weil sie bei vielen Patienten mit OAB-Symptomen auftritt [28] . Dies veranlasste die Forscher, die akuten Auswirkungen der elektrischen Stimulation während einer urodynamischen Studie zu untersuchen.
Einhundertsechsundvierzig Patienten mit idiopathischer Detrusorinstabilität (IDI), sensorischem Drang oder DO als Folge neurogener Erkrankungen zeigten Verbesserungen des MCC ( p = 0,0009) im Vergleich zu den Kontrollen (ohne Stimulation), wenn die Stimulation im Verlauf von S 3 Dermatome [ 29] . In ähnlicher Weise haben Hasan et al. [12] Stimulation im Vergleich zur gleichen Scheinstelle und Kontrollgruppe. Der Vergleich von suprapubischer, sakraler und Scheinstimulation durch Bower et al. [23] diese unmittelbaren Auswirkungen auf MCC nicht eindeutig nachgewiesen haben. Die Autoren schlussfolgerten, dass die beobachtete Verbesserung des First Void Craving (FDV) bei Patienten möglicherweise nicht funktionell wichtig ist, obwohl eine signifikante Verringerung des maximalen Detrusordrucks auf eine potenzielle Wirksamkeit bei DO hindeuten könnte. Ein anderer Ansatz verwendete konditionale Stimulation zur Unterdrückung von Blasenkontraktionen bei 12 MS-Patienten mit detrusor neurogener Überaktivität (NDO) an einer Kreuzbeinstelle [30] und bei acht MS-Patienten im PTN [31] mit einer Nadelelektrode. Leider hatte keiner dieser Patienten ein positives Ansprechen auf die dorsale Penisstimulation, bei der 10/12 Patienten in der Lage waren, die Detrusorkontraktion zu unterdrücken [30] . Der Nervus dorsalis des Penis ist eine Abteilung des Nervus pudendus, und ähnliche Effekte der elektrischen Stimulation wurden bei der Stimulation des Nervus pudendus in beiden anderen Studien am Menschen nachgewiesen [32] und [33] und in Katzen-Tiermodellen [34] und [35] . Dieser Nerv ist ein Nerv tief in der Beckenregion. Es wurde jedoch vorgeschlagen, dass es mit Oberflächenelektroden und einer spezifischen Stimulationswellenform gezielt eingesetzt werden könnte[34] und [35] Wir konnten die Vorteile dieser Wellenform gegenüber einer herkömmlichen Stimulationswellenform demonstrieren [36] . Es scheint also, dass dieser Nerv derzeit nur mit Nadelelektroden angegriffen werden kann.
Ähnlich widersprüchliche Effekte gelten für akute TPTNS-Studien, obwohl Amarenco et al. [37] berichteten bei der Hälfte der untersuchten Patienten mit neurologischen Erkrankungen (MS, Querschnittlähmung, Parkinson-Krankheit) über positive Ergebnisse. Diese Patienten zeigten eine 50%ige Volumenverbesserung bei der ersten Detrusor- und/oder MCC-Kontraktion von mehr als 50% des Ausgangswerts. Eine frühere urodynamische Studie zeigte bei 36 Patienten mit Detrusorhyperaktivität keine signifikanten Unterschiede in einem der urodynamischen Parameter [12] . Dieses unterschiedliche Ergebnis könnte möglicherweise auf unterschiedliche Pathologien zurückzuführen sein, die bei den Patienten beobachtet wurden.
Keiner der beiden Ansätze zur Suche nach akuten Wirkungen, sei es an einem stimulierenden Ort, hat seine Wirksamkeit klar und eindeutig nachgewiesen. Die ausgewogene Literatur deutet jedoch darauf hin, dass Patienten von neuromodulatorischen Effekten profitieren können, die sich aus wiederholten Stimulationssitzungen und nicht aus einer einzigen Anwendung ergeben können. Darüber hinaus haben de Seze et al. [19] kam zu dem Schluss, dass die Behandlung auch bei Patienten wirksam sein kann, die nicht auf eine anfängliche akute TTNS angesprochen haben, die während urodynamischer Tests angewendet wurde.
4. Diskussion
4.1. Welche Stimulationsparameter?
Die Literatur zu den verwendeten Stimulationsparametern ist in Tabelle 1, Tabelle 2 und Tabelle 3 zusammengefasst. Die Lage der Elektroden und der Bereich der Stimulusparameter dürften bei allen Formen der Stimulation kritische Faktoren sein. Zu den relevanten Stimulusparametern gehören die Pulsbreite; Puls-Wiederholungsrate; Burst-Länge (falls zutreffend) und Intensität des Stimulus (vorzugsweise als Strom bezeichnet, da die Spannungsstimulation in Verbindung mit einer unsicheren Impedanz-Elektroden-Gewebe-Schnittstelle zu Unsicherheit hinsichtlich der Stärke des bereitgestellten Stimulus führt). Die technische Beschreibung der in einigen Studien verwendeten Stimuli enthält nicht alle diese Details.
Tabelle 1.
Literaturrecherche zu den klinischen und urodynamischen Wirkungen von TENS während der Langzeitanwendung.
Referenz | Diagnostik/Patientencharakteristika | n | Ort | Impuls-Parameter Stimulus | Behandlungsschema | Klinische Verbesserung (% der Patienten) | Urodynamische Auswertung | ||
Frequenz | Pulsdauer | Intensität | |||||||
McGuire et al. 1983 [16] | MS, SCI, Knickdetrusor, IC | 22 | PTN / Nervus peroneus communis | - | - | - | - | 80% wurden nach der Behandlung trocken oder besserten sich | - |
Hasan et al., 1996 [12] | TUE ICH | 59 | S 2 -S 3Dermatome, perianal | 50 Hz | 200 ms | kitzelndes Gefühl | 2-4 W, 2 Gruppen | Harndranginkontinenz 69 %, Enuresis 73 %, Harndrang 37 % (alle definiert als 50 % Nutzen) | MCC. Volumen abgebrochen, keine Kontraktionen von instabil signifikant verbessert |
Okada et al., 1998 [26] | DH, UID | 19 | Oberschenkelregion | 30 Hz, Modell | 200 ms | Max. unter Schmerzen | 2 W, 1/D, 20 Min | 32% bei Harninkontinenz und Häufigkeit | 11/19 MCC-Patienten nehmen um mehr als 50% zu |
Walsh et al., 1999 [13] | Refraktäres IVD | 32 | S 3Dermatome | 10 Hz | 200 ms | - | 1 W, 1/T, Tag 12 ha | 76 % in der Häufigkeit, 56 % Verringerung der Nykturie, Dringlichkeit Symptom-Score im VAS nicht signifikant verbessert | - |
Skeil et al., 2001 [15] | Neurologisch | 34 | Sakrale Dermatome | 20 Hz | 200 ms | Komfortables Niveau | 6 W, 2 / Tag, 90 min | Signifikante Verbesserung der Inkontinenzepisoden und -häufigkeit | Nicht wesentlich verändert |
Soomro et al., 2001 [14] | IDES | 43 | S 3Dermatome | 20 Hz | 200 ms | kitzelndes Gefühl | 6 mit bis zu 360 min täglicher Verfahrzeit | 56 % Verbesserung der Anzahl der täglichen Voids um mehr als 25 % | Keine merkliche Veränderung gegenüber dem Arm der Stimulationsstudie |
Svihra et al., 2002 [17] | OAB | 28 | PTN | 1 Hz | 100 ms | 70 % Ansprechverhalten des Motors | 5 s, 1/w, 30 min, 3 Gruppen, Steuerung | 56% der Fragebögen bewerten, Kontrollgruppe kein Diff-Zeichen. | - |
Yokozuka et al., 2004 [11] | Neurogene, instabile Blase, Nykturie | 18 | Sakral S 2-S 4Dermatome | 20 Hz 10 s bis 5 s aus | 300 ms | Analer Schließmuskel. | 4 W, 2 / Tag, 15 min | 55 % verbesserte UUI und Frequenz | 44 % erhöhtes MCC und hemmte die Kontraktion |
Bellette et al., 2009 [20] | Nicht-neurogene OAB, Frauen | 37 | PTN | - | - | - | 8 S, 2/W, Scheingruppe | Häufigkeit und Dringlichkeit verbesserten sich in beiden Gruppen signifikant | - |
Schreiner et al., 2010 [18] | UUI, die älteren Frauen | 51 | PTN | 10 Hz | 200 ms | Eine gewisse motorische Reaktion | 12 s, 1/w, 30 min, Steuerung | Die UUI verbesserte sich signifikant in 76 % Vs 26,9 % der Patienten in der Kontrollgruppe | - |
de Seze et al. 2011 [19] | FRÄULEIN | 70 | PTN | 10 Hz | 200 ms | Untermotorisches Ansprechverhalten | 3 m, 1 / Tag, 20 min | 83,3 % verbesserten die Dringlichkeit basierend auf Zeit, MHU-Subskalendringlichkeit und Warnhäufigkeit | Keine Summe. der Patienten mit Detrusor-Hyperaktivität (86 %) sank signifikant auf 73 % |
Booth et al. 2013 [45] | Blase / Schwellkörper, ältere Menschen | 30 | PTN | 10 Hz | 200 ms | Komfort-Level | 12 s, 2/w, 30 min, Scheingruppe | Häufigkeit: 74% Vs. 42% in Fälschung | - |
DH, hyperreflexiver Detrusor; IC, interstitielle Zystitis; IDI, idiopathische Detrusorinstabilität; IDO, idiopathische Detrusor-Hyperaktivität; IVD, irritative Entleerungsstörungen; MCC, maximale Zystometrie-Kapazität; MHU, Mesure du Handicap urinaire; MS, Multiple Sklerose; OAB, überaktive Blase; PTN, Nervus tibialis posterior; Querschnittlähmung, Rückenmarksverletzung; SU, sensorische Dringlichkeit; UUI, Harndranginkontinenz.
Optionen für Tabellen
Tabelle 2.
Literaturrecherche zu den akuten urodynamischen Wirkungen von TENS.
Erstes Jahr der Autorenschaft | Diagnose | n | Ort | Impuls-Parameter Stimulus | Details zur Studie | Urodynamisches Ergebnis | ||
Frequenz | Pulsdauer | Intensität | ||||||
Hasan et al., 1996 [12] | IDES | 36 | Suprapubische PTN | 50 Hz | 200 ms | kitzelndes Gefühl | Teil der großen Studie | Kein signifikanter Unterschied in einem der Parameter |
59 | S 2 -S 3 T 12(Schein) Steuerung | 50 Hz | 200 ms | kitzelndes Gefühl | 3 Gruppen, Fiktion, Kontrolle | MCC signifikant erhöht in S 2 -S 3 Stimulation im Vergleich zu Täuschung und Kontrolle | ||
Bower et al., 1998 [23] | VON, AUF | 79 | sakral | 10 Hz | 200 ms | Max. tolerierbare Empfindung | 3 Gruppen, Sham | max. DP- und FDV-Steigerung |
suprapubisch | 150 Hz | 200 ms | max. DP- und FDV-Steigerung | |||||
Fiktion | Kein Stimulus | Anstieg der MCC auf Su pts. | ||||||
Walsh et al., 2001 [29] | IDI, SU, DH (SKI, MS) | 146 | Perianale Dermatome | 10 Hz | 200 ms | - | Kontrollgruppe | FDV ( p = 0,002) und MCC ( p = 0,0009) ist im Vergleich zur Regelung |
Amarenco et al., 2003 [37] | MS, SCI, PD, IDI | 44 | PTN | 10 Hz | 200 ms | Untermotorisches Ansprechverhalten | Akute Wirkung | 48 % (21/44) erhöhtes Volumen bei FIDC, 34 % (15/44) erhöhte MCC |
Fjorback et al., 2007 [30] | FRÄULEIN | 12 | sakral | 20 Hz | 500 ms | 50-60 mA | Bedingte Stimulation | 0/12 konnten die Kontraktion des Detrusors unterdrücken |
DPN | 20 Hz | 500 ms | 50-60 mA | 10/12 konnten die Kontraktion des Detrusors unterdrücken | ||||
DH, hyperreflexiver Detrusor; DI, Knickdetrusor; DPN, dorsaler Penis/Klitorisnerv; FDV, erster Harndrang; FIDC, erste unwillkürliche Kontraktion des Detrusormuskels; IDI, idiopathische Detrusorinstabilität; MCC, maximale Zystometrie-Kapazität; MS, Multiple Sklerose; Parkinson, Parkinson-Krankheit; PTN, Nervus tibialis posterior; Querschnittlähmung, Rückenmarksverletzung; SU, sensorische Dringlichkeit.
Optionen für Tabellen
Tabelle 3.
Zusammenfassung der Studien, die nach Art und Ort der Stimulation überprüft wurden.
Nicht-Kontrolle | Placebo-Kontrolle | Andere Form der Kontrolle | |
sakral | Yokozuka et al. [11] | Bower et al. [23] | Fjorback et al. [30] |
PTNS (PTNS) | Amarenco et al. [37] | Booth et al. [45] | Schreiner et al. [18] |
Suprapubisch / Sonstiges | Okada et al. [26] | Bower et al. [23] | Hasan et al. [12] |
Optionen für Tabellen
Um eine sakrale Stimulation zu erreichen, haben Yokozuka et al. [11] Patienten, die die Aufgabe hatten, Oberflächenelektroden auf dem Foramen sacralis posterior zu platzieren und die Intensität der Stimulation bis zu einer analen Kontraktion zu erhöhen, konnten ertastet werden. Sie stellten die Hypothese auf, dass in Fällen, in denen keine Besserung eintrat, die Elektroden nicht in der richtigen Position platziert wurden oder die Intensität aufgrund der damit verbundenen Beschwerden nicht hoch genug war. Es gibt Unterstützung für Takahashi und Tanaka [38] bei denen geringfügige Veränderungen in der Position der Elektroden zu spürbaren scheinbaren Veränderungen der Harnröhrendruckantwort führten [11] . Bei den bisher berichteten Studien zur sakralen Stimulation werden in der Regel Elektroden in Sakrallöchern oder am Gesäß über dem S platziert 2 und S 3Dermomen. Die genaue Platzierung von Elektroden an heiligen Stätten variiert zwischen den Studien, vermutlich weil die Lage der sakralen Dermatome unsicher ist [39] und [40] . Die Intensität des Reizstroms wurde in der Regel auf ein Maximum eingestellt, das von der Schmerzschwelle vorgegeben wurde. In anderen Studien wurden die Patienten angewiesen, eine Intensität einzustellen, die ein kitzelndes Gefühl hervorrief [12] , [14] und [15] . Nervenstämme (Wurzeln) in diesen Bereichen befinden sich tief in den Foramina und es ist unwahrscheinlich, dass diese direkt bei der Intensität des verwendeten Reizes stimuliert wurden. Die Hautnerven in Dermatomen sind jedoch leicht zu stimulieren, so dass eine oberflächliche sensorische Faserstimulation, die sowohl zu einer direkten als auch zu einer indirekten Modulation der Reflexmechanismen des Rückenmarks führen kann, die berichteten Effekte erklären kann. Darüber hinaus ist die Intensität, die eine Kontraktion des Analschließmuskels hervorruft, [11] Es handelt sich um die Stimulation der motorischen Nerven, wodurch verschiedene Mechanismen aktiviert werden, und kann den Patienten erhebliche Beschwerden bereiten. Die Klärung des genauen Stimulationsortes und der erforderlichen Intensität sollte in zukünftigen Arbeiten angegangen werden. Basierend auf der verfügbaren Evidenz sind wir nicht in der Lage, zu entscheiden, welche die besten Stimulationsparameter für die sakrale Stimulation sind. Die ursprüngliche Beschreibung von PTNS durch McGuire et al. [16] Sie wurde in Bezug auf die Position der Elektroden nicht wiederholt. In den meisten Studien werden die Elektroden in der Nähe des medialen Knöchels platziert, wo die PTN relativ flach ist. Es ist unklar, auf welchem Bein die Elektroden platziert werden müssen, um eine optimale Reaktion zu erzielen, und ob dies wichtig ist. Einige Autoren platzierten Elektroden am linken Bein [17] , [20] und [37] , während andere am rechten Bein [18] , [19] und [31] . Es kann auch effektiver sein, Elektroden bilateral zu platzieren, obwohl dies noch keine Studien untersucht haben. Bei der Beschreibung der aktuellen Intensitätseinstellung stellten einige der Studien motorische Reaktionen während der Stimulation dar [17] und [18] . In anderen Studien wurde die Stimulationsintensität knapp unter der motorischen Schwelle eingestellt [37] oder knapp über der Wahrnehmungsschwelle [19] .
Die Studie, die über die vielversprechendsten therapeutischen Ergebnisse berichtet, ist die von de Seze et al. [19] , die über den Erfolg von PTNS bei OAB-Symptomen bei MS-Patienten berichtet hat. Die Stimulationsintensität lag in dieser Studie hinter der Wahrnehmungsschwelle und die Patienten berichteten über keine motorischen Reaktionen nach der Stimulation. Daher wurden wahrscheinlich nur sensorische Fasern oder Hautnerven stimuliert, die über dem PTN liegen, was darauf hindeutet, dass dies für die Behandlung von OAB ausreichend sein könnte. Wenn die Behandlung selbst verabreicht wird, ist es wahrscheinlich, dass der Patient niedrigere Stimulationsniveaus bevorzugt, was dann zu einer Stimulation der Hautnerven allein und nicht des hinteren Tibialisnervs selbst führen kann.
4.2. Schein-Stimulations-Methodik
Die Erforschung möglicher Placebo-Effekte ist wahrscheinlich bei der Erforschung neuer Therapien unerlässlich, und dies ist insbesondere bei elektrischen Stimulationstechniken der Fall, da sie Empfindungen hervorrufen. Aufgrund dieser Empfindungen kann die Produktion einer vorgetäuschten elektrischen Stimulation jedoch schwierig sein. Eine interessante Methodik wurde in einer Studie mit Kindern mit OAB durchgeführt, bei der in einem Arm der Studie eine Stimulation über das Schulterblatt angewendet wurde, wo Auswirkungen auf die Kontrolle der unteren Harnwege zu erwarten sind [41] . In ähnlicher Weise haben Hasan et al. [12] TENS über dem T 12 Dermatom, das als Placebo wirkte.
Elektrische Stimulation unterhalb der motorischen Schwelle verursacht Kribbeln aufgrund der Stimulation der sensorischen Nervenstrukturen der Haut. Eine alternative Option für eine Scheinmethode kann darin bestehen, die Stimulationsintensität nach einigen Sekunden der Anwendung allmählich auf Null zu verringern und dem Probanden anzuzeigen, dass die Empfindungsreize mit der Zeit nachlassen können. Dies ist ein Ansatz, der in Techniken wie der transkraniellen Stromstimulation weit verbreitet ist [42] . Darüber hinaus kann es sein, dass sich der Proband an solche Reize anpasst, dass er nicht wirklich erkennen kann, ob die Stimulation anhält oder nicht. Diese Gewöhnung hängt wahrscheinlich von der Häufigkeit der verwendeten Stimulation, der Stärke der angewendeten Reize und von den persönlichen subjektiven Reaktionen ab.
Ein weiterer Ansatz bei Placebo-Effekt-Untersuchungen könnte darin bestehen, Elektroden auf die gleiche Hautstelle aufzubringen, jedoch ohne Stimulationsstrom mit dafür modifizierten Stimulatoren [43] . Dies setzt jedoch voraus, dass der Patient in Bezug auf die elektrische Stimulation naiv sein muss und daher nicht weiß, dass sie Empfindungen hervorruft.
Leroi et al. [44] Es wurde eine randomisierte, scheinkontrollierte Studie durchgeführt, in der den Patienten nicht mitgeteilt wurde, dass sie die Scheinstimulation erhalten könnten. Die Patienten wurden randomisiert in aktive und Schein-Stimulus-Gruppen eingeteilt. Diese Methodik wurde von der örtlichen Ethikkommission gebilligt, obwohl die Herausgeber der Zeitschrift, in der sie später veröffentlicht werden, den Forschern dringend davon abraten, eine solche Methode zu verwenden, da sie der Meinung sind, dass sie einen Verstoß gegen die Deklaration von Helsinki darstellen könnte. Wir sind der Meinung, dass dies ein vertretbarer Ansatz ist, um die technischen Probleme der fiktiven Stimuli zu überwinden, die ihm in der Phase der Genehmigung durch die zuständige Ethikkommission ausgesetzt sind. Der Nutzen einer solchen Regelung für den Patienten muss jedoch berücksichtigt werden, und das Angebot einer aktiven Behandlung nach der Studie könnte dieses Problem lösen.
5. Fazit
Die Wahl der Stimulationsparameter, der Ort der applizierten Stimulation, die verwendeten Outcome-Messungen und die untersuchten Grunderkrankungen und Symptome sind in der bisherigen Literatur sehr unterschiedlich. In der Literatur sind nur wenige Langzeit-Follow-up-Daten veröffentlicht, so dass das Behandlungsschema unklar ist, um einen anhaltenden Nutzen zu erzielen.
Der derzeitige Konsens ist, dass die vielversprechendste Stimulationsstelle S ist 3 Bereich des Rückenmarks in der Sakralregion oder oberhalb des hinteren Tibianervs, aber es ist unklar, welcher Reizabgabeansatz der effektivste ist. Über die Wirkmechanismen, die dem Wirken zugrunde liegen, ist wenig bekannt und es müssen genaue Strukturen stimuliert werden.
Es gibt jedoch verlockende Beweise für die Wirksamkeit des transkutanen Stimulationsansatzes, obwohl weitere große placebokontrollierte Studien erforderlich sind, um eine solide Wissensbasis zu schaffen. Die Standardisierung der zukünftigen Prozessmethodik ist wichtig, um Vergleiche zwischen Studien und Stimulationsprotokollen zu ermöglichen.
Leistungsbeschreibung:
- Stromversorgung: 2 x 1,5 V AA Alkaline-Batterien (LR6);
- Ausgang: 100 mApp an 1000 Ohm Last (mit 200mS Impulsen)
- Pulsbreite: 50mS bis 400mS einstellbar in 50mS-Schritten
- Frequenz: 1 Hz bis 150 Hz (1-2-3-4-5-10-12-14-16-18-20-25-30-35-40-45-50-60-70-80-90-100-110-120-130-140-150).
- Wellenform: symmetrische zweiphasige Impulse - abwechselnde zweiphasige Impulse.
- Behandlungs-Timer: Kontinuierlich, 10min, 20min, 30min, 45min, 60min, 90min.
- AKTIONS-/PAUSENZEITEN: Von 1 bis 60 Sek., einstellbar in Schritten von 1 Sek.
- RAMP-Zeit: Von 0 bis 5 Sek., einstellbar in Schritten von 1 Sek.
- Abmessungen: 138 mm x 6 8 mm x 28 mm.
- Gewicht: 160 g. Batterien im Lieferumfang enthalten.
- Betriebs- und Lagertemperatur: von +5 bis +35 °C.
- Relative Luftfeuchtigkeit bei Gebrauch und Lagerung: von 20 % bis 80 %.
Ausrüstung:
- Intellistim BE-28UG Gerät
- 2 Taststift-Akkus
- Anschlusskabel
- Benutzerhandbuch in englischer Sprache
- Reisekoffer
Sonden sind separat zu erwerben.